Mechanismus entdeckt, wie das Coronavirus die Zelle kapert
Forschende der Universität Bern und der ETH Zürich haben einen Mechanismus entdeckt, wie das Coronavirus menschliche Zellen manipuliert, um seine eigene Vermehrung sicherzustellen. Dieses Wissen wird helfen, Medikamente und Impfstoffe gegen das Coronavirus zu entwickeln.
Wie ein Pirat, der ein Schiff kapert, übernimmt ein Virus die Kontrolle über eine infizierte Zelle, denn jedes Virus ist für seine Vermehrung auf die Ressourcen und molekularen Maschinen der Zelle angewiesen. Das gilt auch für Sars-CoV-2, den Auslöser der Covid-19-Pandemie. Forschende der Universität Bern und der ETH Zürich haben nun einen Mechanismus entdeckt, den das Coronavirus benutzt, um die Herstellung seiner Proteine gegenüber den zelleigenen zu bevorzugen. Dieser Mechanismus führt dazu, dass die Zellen die Produktion der eigenen Proteine stark reduzieren und stattdessen fast nur noch Virusproteine produzieren. So wird nicht nur die Produktion neuer Viren angeregt, sondern auch die Immunantwort gegen die Coronainfektion gehemmt.
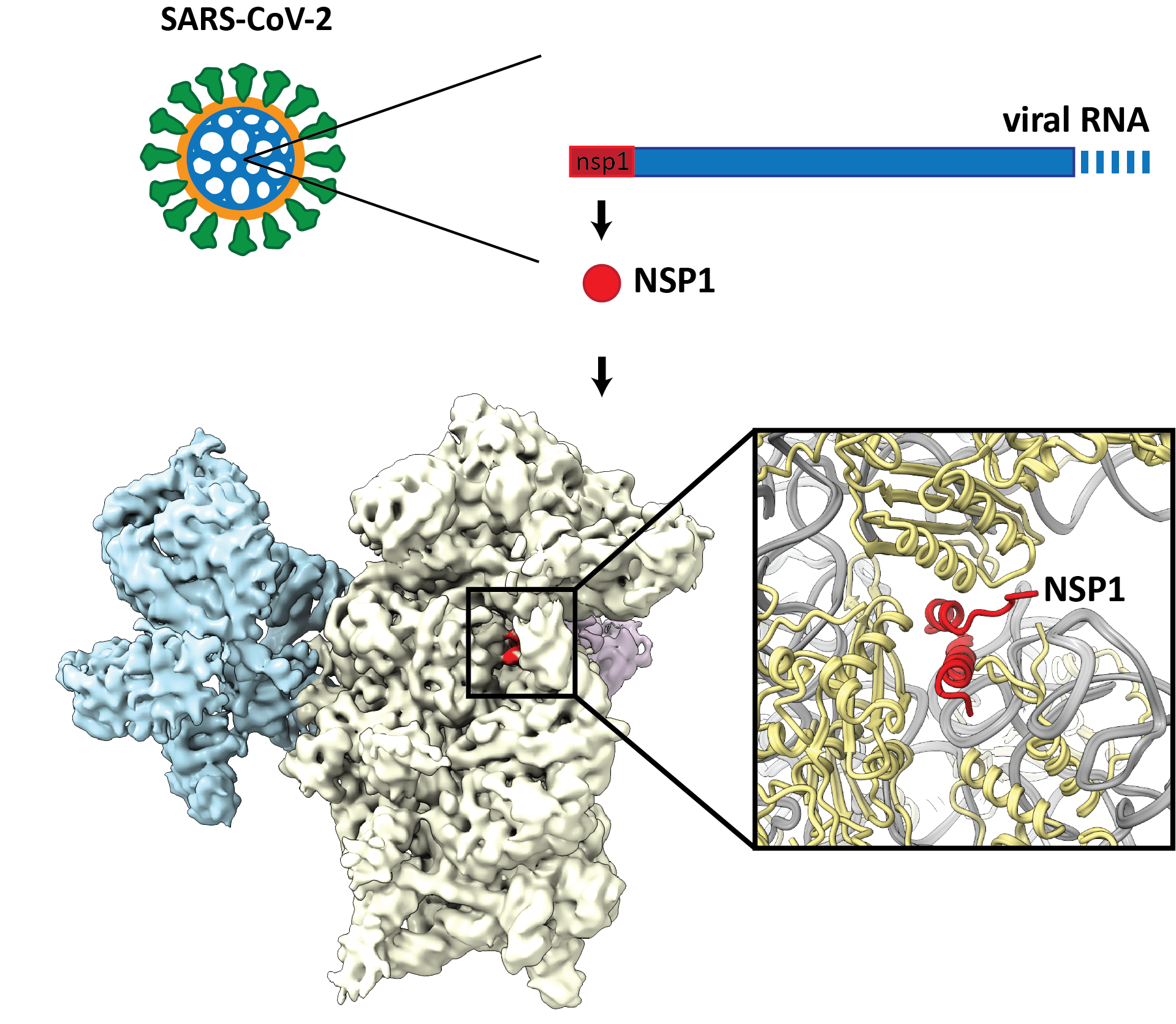
Nachdem bei einer Sars-CoV-2 Infektion das Virus in eine menschliche Zelle eingeschleust wurde, wird das Protein NSP1 als eines der ersten Virusproteine hergestellt. Von anderen Coronaviren wusste man bereits, dass NSP1 die Produktion von zelleigenen Proteinen hemmt, jedoch war bisher nicht bekannt, wie dies geschieht. Nun haben die Forschenden der Universität Bern und ETH Zürich herausgefunden, wie NSP1 die zelluläre Proteinproduktion hemmt. Diese Arbeit wurde nun veröffentlicht. Sie ergänzt die Erkenntnisse, welche ein anderes Forscherteam aus Deutschland jüngst publizierte.
Viraler Mechanismus als Ansatzpunkt für die Impfstoff- und Medikamentenentwicklung
Ribosomen sind die zellulären Maschinen, welche Proteine herstellen. Dazu lesen sie den Bauplan, die sogenannte Boten-RNA, für ein gegebenes Protein ab und fügen die Aminosäuren in der entsprechenden Reihenfolge zusammen. Beim Ablesen passiert die Boten-RNA einen Kanal im Ribosom. Die Forschenden konnten zeigen, dass NSP1 innerhalb des Kanals bindet und so das Ribosom blockiert. Mittels der Kryo-Elektronenmikroskopie konnte die Bindungsstelle von NSP1 mit atomarer Auflösung dargestellt werden. «Dieses detaillierte Abbild liefert wichtige Informationen zum Design eines möglichen künftigen Medikamentes, welches die Bindung von NSP1 verhindert, die ribosomale Funktion aber nicht beeinträchtigt. Wenn NSP1 nicht mehr mit dem Ribosom interagieren kann, wird die zelluläre Immunantwort angeregt und die Virusvermehrung gestoppt», erläutert Nenad Ban, Professor für Molekularbiologie an der ETH Zürich und Mitautor der Studie.
Mittels biochemischer und zellulärer Experimente konnten die Forschenden zeigen, dass NSP1 allein genügt, um die Proteinproduktion zu hemmen. Basierend auf dem detaillierten Abbild der Bindungsweise von NSP1 konnten sie abgeänderte NSP1 Varianten herstellen, die ihre hemmende Wirkung verloren haben. Sars-CoV-2 Viren mit solchen inaktiven Varianten des NSP1 Proteins würden so abgeschwächt sein, dass sie sich nicht mehr vermehren und somit auch keine starke Krankheit mehr auslösen können. Solche abgeschwächten, inaktiven Viren können als Impfstoff verwendet werden; ein Prinzip, auf dem bereits viele andere Impfungen gegen Viruskrankheiten basieren.
Weiterhin interessierte die Forschenden die Frage, warum die Virenproteine in grossen Mengen hergestellt werden – trotz der Hemmung der Ribosomenfunktion durch NSP1. Sie fanden heraus, dass die virale RNA die Eigenschaft hat, verglichen zu den zellulären Boten-RNAs, sehr effizient von den Ribosomen abgelesen zu werden. «Durch die Blockierung von Ribosomen durch NSP1 werden funktionsfähige Ribosomen knapp, und gleichzeitig kann die virale RNA fast die Hälfte der gesamten RNA in der Zelle ausmachen. Unter diesen Bedingungen wird die virale RNA von den noch funktionsfähigen Ribosomen gegenüber den zelleigenen Boten-RNAs bevorzugt abgelesen», erklärt Oliver Mühlemann, Professor für Biochemie an der Universität Bern und ebenfalls Mitautor der Studie.
Forschungsprojekt in Rekordzeit
Von Beginn des Forschungsprojektes bis zur Publikation sind nur wenige Monate vergangen. «Die komplementäre Expertise der beteiligten Forschenden erlaubte ein sehr schnelles und effizientes Vorankommen in diesem Projekt», sagt Oliver Mühlemann. Alle drei beteiligten Forschungsgruppen sind Teil des Nationalen Forschungsschwerpunktes NCCR RNA & Disease des Schweizerischen Nationalfonds, bei dem die Universität Bern Leading House und die ETH Zürich Co-leading House ist. Die drei Forschungsgruppen werden weiterhin eng zusammenarbeiten, um weitere Erkenntnisse darüber zu gewinnen, wie Sars-CoV-2 die Zelle zu eigenen Gunsten manipuliert.
NCCR RNA & Disease – Die Rolle von RNA in KrankheitsmechanismenDer Nationale Forschungsschwerpunkt (NCCR) «RNA & Disease – Die Rolle von RNA in Krankheitsmechanismen» widmet sich der Untersuchung einer sehr zentralen Klasse von Molekülen. Die RNA (Ribonukleinsäure) ist der Drehpunkt vieler Lebensvorgänge und funktional weit vielfältiger als ursprünglich angenommen. Sie definiert beispielsweise, wann und in welchen Zellen welche Gene aktiv oder inaktiv sind. Läuft bei dieser genetischen Regulation nicht alles rund, entstehen Krankheiten – etwa Herzerkrankungen, Krebs, Hirn- und Stoffwechselkrankheiten. Der NCCR vereint Schweizer Forschungsgruppen, die sich mit verschiedenen Aspekten der RNA-Biologie befassen. Indem der NCCR aufdeckt, welche regulatorischen Mechanismen während einer Erkrankung aus dem Ruder laufen, zeigt er auch neue therapeutische Angriffsziele auf. Die Universität Bern ist Leading house des NCCR, die ETH Zürich ist co-leading. Nationale Forschungsschwerpunkte sind ein Forschungsinstrument des Schweizerischen Nationalfonds SNF. |
Publikationsdetails:Katharina Schubert, Evangelos D. Karousis, Ahmad Jomaa, Alain Scaiola, Blanca Echeverria, Lukas-Adrian Gurzeler, Marc Leibundgut, Volker Thiel, Oliver Mühlemann & Nenad Ban: SARS-CoV-2 Nsp1 binds the ribosomal mRNA channel to inhibit translation. Nature Structural & Molecular Biology (2020), https://doi.org/10.1038/s41594-020-0511-8 |
14.09.2020